前言
美国芝加哥当地时间5月31日~6月4日,第55届美国临床肿瘤学会(ASCO®)拉开帷幕。2019年6月2日召开的全体大会专场(Plenary Session)可谓万众瞩目的焦点,会上公布了由ASCO学术委员会从全部摘要中挑选出的4项延迟公布摘要(Late Breaking Abstract),是公认的本年度最重要的研究,被认为能够改变临床实践。

其中现场公布的LBA4摘要报道了在一线铂类化疗后未进展、携带胚系BRCA(gBRCA)突变的转移性胰腺癌(mPDAC)患者中奥拉帕利维持治疗疗效的POLO研究的重要结果,证实了PARP抑制剂作为维持治疗能够显著延长mPDAC患者的无进展生存期(PFS)且安全性良好,在减缓患者疾病进程的同时未对患者生活质量产生不良影响。美国当地时间6月2日,POLO研究结果全文同步发表于《新英格兰杂志》(NEJM)。

中国医学论坛报记者第一时间邀请我国胰腺癌领域权威专家解放军东部战区总医院全军肿瘤中心主任秦叔逵教授、复旦大学附属肿瘤医院胰腺外科主任虞先濬教授以及上海交通大学医学院附属仁济医院肿瘤科主任王理伟教授对POLO研究结果及对胰腺癌临床实践的影响进行点评,以期让广大读者实时掌握研究动态,了解研究传递传递的重要信息。
专家点评

全国政协委员、解放军东部战区总医院全军肿瘤中心主任 秦叔逵教授
(兼任《临床肿瘤学杂志》主编、中国临床肿瘤学会(CSCO)副理事长、CSCO胰腺癌专委会副主任委员和胰腺癌指南编写组副主编)
秦叔逵教授:胰腺癌是临床常见的消化系统恶性肿瘤,高度侵袭、进展迅速,易于转移,治疗极为艰难。80%的胰腺癌,诊断时已达局部晚期或者发生转移,预后恶劣,5年生存率始终徘徊在10%以下。多年来,肿瘤学界和医药界对晚期患者的系统性药物治疗不断探索,从5-FU到S-1,再到FOLFIRINOX方案,从吉西他滨到吉西他滨联合白蛋白紫杉醇,进步比较缓慢,生存获益有限,而分子靶向治疗和免疫治疗的研究虽不断开展,但是屡屡失败,“油盐不进”,面临窘境。终于石破天惊,在本次ASCO大会上公布的POLO研究获得了成功,引起轰动。
POLO研究结果表明,对于具有gBRCA突变的晚期转移性胰腺癌患者,在一线含铂化疗之后,釆用PARP抑制剂奥拉帕利维持治疗,相比安慰剂对照组显著延长了无进展生存(mPFS: 7.4个月对3.8个月;HR=0.53),即使得疾病进展风险降低了47%。随访一年后,奥拉帕利治疗组患者中有33.7%无疾病进展,而安慰剂组仅为14.5%;两年后,奥拉帕利组患者中22.1%无疾病进展,而安慰组仅为9.6%。由此晚期胰腺癌的临床治疗模式将发生重大变革。
未来应该积极推荐在胰腺癌患者确诊时就进行基因组学检测,特别是针对BRCA突变的检测。gBRAC突变阳性的晚期胰腺癌患者,推荐一线使用含铂化疗方案,并考虑在一线含铂化疗后将PARP抑制剂作为标准的维持治疗药物。
POLO研究成为全球第一项依据生物标记物针对晚期胰腺癌实施精准治疗获得成功的大型III期临床研究,独领风骚,提示我们应该重视胰腺癌的分子分型和靶向干预问题,进一步深入探索。另外,还需要思考对于BRCA突变之外的胰腺癌患者,如何进行研究,以明显改善治疗获益。

上海市/复旦大学胰腺肿瘤研究所所长、复旦大学附属肿瘤医院胰腺外科主任 虞先濬教授
[兼任中国抗癌协会胰腺癌专业委员会候任主任委员、中国抗癌协会胰腺癌专业委员会多学科临床研究协作学组CSPAC组长、牵头执笔胰腺癌综合诊治指南(2018版)]
虞先濬教授:POLO的研究结果振奋人心,奥拉帕利作为首个在胰腺癌中经III期临床研究验证的PARP抑制剂靶向药物,标志着biomarker-driven治疗时代在胰腺癌领域正式开启,具有里程碑意义,且再次强调了筛选人群的重要性及维持治疗理念的意义。
2011年PRODIGE4-ACCORD11研究奠定了FOLFIRINOX对体力评分好的mPDAC患者的一线治疗地位(mOS 11.1个月, mPFS 6.4个月, 对比吉西他滨单药);POLO III期研究中,经一线含铂化疗未进展的患者,后续采用奥拉帕利单药维持,PFS达7.4月,OS达18.9月(对比安慰剂),结果可喜,显著改善了gBRCA突变胰腺癌人群(4%-7% )的生存及预后。
2019年NCCN-V2意见将FOFIRINOX、吉西他滨+顺铂作为BRCA1/2或PALB2突变的体力状态较好胰腺癌患者的推荐化疗方案(不论新辅/局部晚期/转移性);但关于这类人群治疗的研究并不多,推荐基于小样本数据。而PARP抑制剂的应用,有望为此类分子分型的胰腺癌患者带来新的治疗局面。
尽管奥拉帕利目前适应证局限,但后续临床扩展空间广阔,包括用于其他同源重组修复缺陷相关的胚系/体细胞突变(ATM、PALB2等),铂类单药联合PARP抑制剂维持治疗方案,联合其他治疗如免疫检查点抑制剂,前移至新辅助、辅助、晚期一线方案的可能性等。此外,因奥拉帕利不良反应而中断治疗、减量或退出的比例分别为39.6%(32/91)、15%(16.5/91)以及5%(5.5/91),因此临床需提高对奥拉帕利不良反应的管理,努力改善胰腺癌患者健康相关生命质量。

上海交通大学医学院附属仁济医院肿瘤科主任 王理伟教授
(上海交通大学胰腺癌诊治中心主任,兼任CSCO胰腺癌专家委员会主任委员、中华医学会肿瘤学分会委员兼胰腺肿瘤学组组长)
王理伟教授:多数胰腺癌患者初诊时就已经失去手术治疗机会,转移性胰腺癌的治疗在近年来虽有进展但标准治疗药物的选择依旧停留在5-FU类和吉西他滨为主的化疗方案。FOLFIRINOX 标准方案和吉西他滨联合白蛋白紫杉醇分别带来了 11 个月和 8.5 个月的中位总生存期,缓解率分别在 31.6%和 23%,且两个方案均存在较大的不良反应,标准治疗后的后续方案选择较为匮乏。2019 年 ASCO 带来的 POLO 研究为捉襟见肘的现状带来改变,基于生物标志物个体化治疗胰腺癌的时代正在徐徐开幕。
在 POLO 研究中,研究者基于前期研究——具有gBRCA突变的mPADC患者一线接受含铂化疗往往效果较野生型患者更好——结合 PARP 抑制剂较好的安全性,将针对 BRCA突变的 PARP 抑制剂应用到胰腺癌的维持治疗中并取得了成功。研究采用了两个严苛且重要的纳入标准,即具有gBRCA突变且需要在一线含铂标准治疗过程中未出现进展,研究中共有 21.7%(43/198) 的患者在一线治疗中出现进展而无法随机化。POLO 研究显示,奥拉帕利维持治疗组获得了7.4 个月的中位PFS,同时带来了生存获益,与安慰剂组相比,奥拉帕利使疾病进展的风险降低了47%(HR= 0.53);一年后,接受奥拉帕利治疗的患者中有33.7%没有出现疾病进展,而接受安慰剂维持的患者仅为14.5%。两年后,接受奥拉帕利治疗的患者中有22.1%无疾病进展,而服用安慰剂的患者为9.6%。
在卵巢癌中,奥拉帕利的适应证从三线治疗失败后治疗到获批一线维持治疗,结合奥拉帕利在这部分胰腺癌患者中的获益,有理由将其角色再次放大。在今后的研究中,奥拉帕利联合铂类药物一线治疗具有胚系 BRCA 突变的转移性胰腺癌患者未尝不可尝试。在未来,随着免疫检查点抑制剂和其他靶向药物研究在胰腺癌中的进展,必然会有更多的药物通过联合甚至像其他瘤种一样单用于胰腺癌的多线治疗中。此外,更为关键的是,POLO研究是胰腺癌中首个基于生物标志物的靶向治疗显著获益的 III 期临床研究,这开启了胰腺癌个体化精准治疗的时代。
研究详情III期POLO研究:探索奥拉帕利作为维持治疗用于一线铂类化疗后未进展、携带gBRCA突变的mPDAC患者
胰腺癌是一类恶性程度高、起病隐匿的恶性肿瘤,绝大多数患者在就诊时已为晚期,由此药物为主的综合治疗在胰腺癌治疗中占据重要地位。近年来,各种靶向药物都在围绕胰腺癌治疗展开探索,期待能够找到更为优化的治疗策略和更多获益的治疗药物。既往研究显示,携带gBRCA1和/或BRCA2突变的胰腺癌患者对PARP抑制剂奥拉帕利治疗表现出应答反应(Kaufman 2015)。为此,研究者开展了POLO研究,以期明确PARP抑制剂这类靶向药物在胰腺癌一线化疗后维持治疗的作用,该研究是评估PARP抑制剂在胰腺癌维持治疗中疗效的首项III期临床试验。
01研究设计
POLO研究是一项国际性、随机、双盲、安慰剂对照III期临床试验,纳入曾接受转移性疾病治疗、在完成至少16周的一线含铂联合化疗(PBC)后未进展的携带gBRCA突变的胰腺癌患者,按3:2的比例随机分配接受奥拉帕利(300 mg,口服,bid)或安慰剂维持治疗。患者在最后一次PBC治疗后4~8周进行随机分组并启动维持治疗,持续至研究者评估的疾病进展或出现不可接受的毒性。研究主要终点为经盲法独立中心评价(改良RECIST 1.1)的PFS;次要研究终点包括总生存期(OS)、全球健康相关生活质量(HRQoL)评分较基线的校正后平均变化、奥拉帕利的安全性和耐受性等。

02研究结果
研究共筛选患者3315例,其中携带gBRCA突变患者247例,对154例患者进行随机分组(奥拉帕利组92例,安慰剂组62例),151例患者接受治疗(奥拉帕利组90例,安慰剂组61例)。患者基线特征见表。

表. 患者基线特征
研究结果发现,经16周一线化疗及后续维持治疗,奥拉帕利组与安慰剂组相比PFS得到显著改善(中位PFS为7.4个月对3.8个月;风险比(HR)为0.53,95%CI 0.35,0.82;P=0.0038,图1),无论既往PBC的缓解情况如何结果保持一致(完全缓解/部分缓解HR=0.62;疾病稳定HR=0.50)。

图1. 奥拉帕利组与安慰剂组的PFS结果
从第6个月起,奥拉帕利组患者的PFS率为安慰剂组患者2倍,且在12个月、18个月和2年评估均为安慰剂组的2倍以上(图2)。
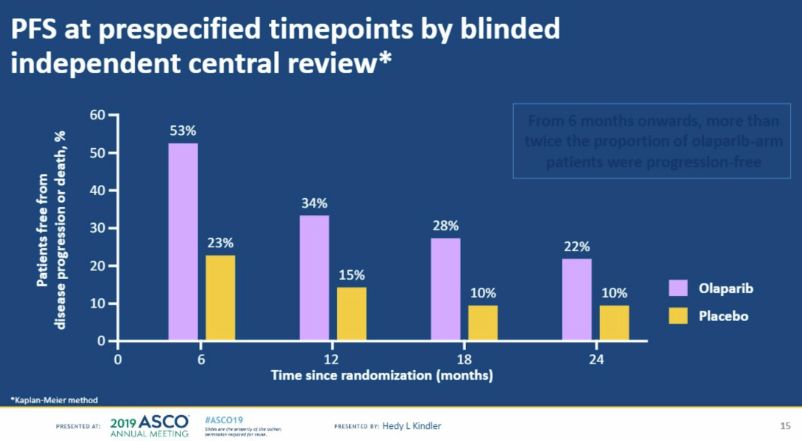
图2. 不同时间点两组患者PFS率
在中期总生存(OS)分析(成熟度46%)中, HR为0.91(95%CI 0.56,1.46;P=0.68)。安全性方面,奥拉帕利组有40%的患者发生了3级或以上不良事件(AE),安慰剂组为23%。奥拉帕利组和安慰剂组分别有5.5%和1.7%的患者因AE停止治疗。在患者报告的生活质量方面,奥拉帕利组HRQoL评分较基线平均变化为-1.20±1.42,安慰剂组为1.27±1.95,两组HRQoL评分较基线未出现具有临床意义的变化。同时,两组间HRQoL评分较基线平均变化的差异并无临床意义。
03研究结论
奥拉帕利维持治疗为一线铂类化疗后未进展、携带gBRCA突变的mPDAC患者带来了具有显著统计学意义和临床意义的PFS改善。中期OS数据(成熟度46%)两组间未见差异,最终OS结果将在数据达到69%成熟度时进行评价。患者对于奥拉帕利维持治疗的耐受性良好,奥拉帕利安全性特征与已知其他瘤种报道一致。此外,奥拉帕利组的健康相关生活质量与安慰剂组相似。POLO研究是首个在生物标志物筛选胰腺癌人群中验证靶向治疗疗效的III期研究,这也表明了gBRCAm检测在该疾病人群中的重要性。
现场点评
会上,科罗拉多大学癌症中心Wells Messersmith教授对POLO研究做现场点评。专家表示,POLO研究中奥拉帕利维持治疗给胰腺癌患者带来的PFS获益令人印象深刻,同时,经由亚组分析可看出,无论患者对一线PBC的应答情况如何(完全缓解、部分缓解或疾病稳定)、携带gBRCA1突变或gBRCA2突变、年龄小于65岁或大于等于65岁,各亚组患者均可从奥拉帕利维持治疗中获得PFS获益。除此之外,在安全性方面,奥拉帕利维持治疗的不良反应可控,与既往PARP抑制剂报道的不良反应相似。
可以说,POLO研究创造了胰腺癌领域的两项“第一”。首先,第一项以生物标志物驱动的胰腺癌临床研究,其次,胰腺癌领域第一项取得成功的维持治疗III期研究。POLO研究表明,对于携带gBRCA突变的转移性胰腺癌患者,奥拉帕利维持治疗或将成为新的治疗选择。